Пошкодження клітинного ядра, спричинене ліпідними пероксидами, має особливо серйозний вплив: це призводить до руйнування клітин, зміни генетичного матеріалу та перетворення у вироджені клітини. Оскільки механізми відновлення клітин також обмежені, пошкодження, спричинені перекисним окисленням ліпідів, неможливо повністю відновити. Це призводить до передчасного та прискореного процесу старіння в організмі.
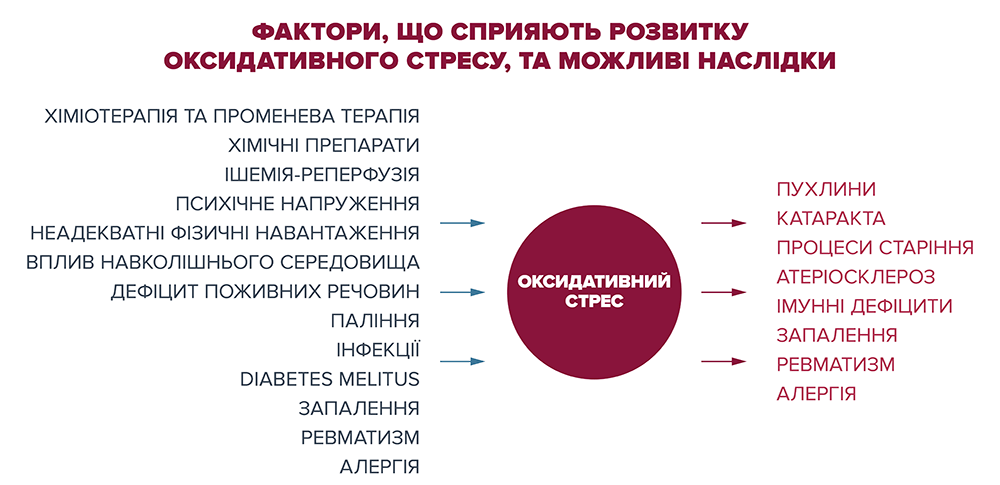
У здоровому організмі існує баланс між прооксидативними факторами та антиоксидативними компонентами, що складаються з ферментів, вітамінів, мікроелементів та амінокислот. Численні хвороби, стреси, забруднення, приймання ліків, а також дієти та шкідливі звички (наприклад, паління) призводять до зміни цього балансу на користь оксидантів. Наслідки цього дисбалансу відомі як “оксидативний стрес”. Він характеризується надмірним утворенням активних форм кисню (наприклад, вільних радикалів), які організм вже не може довготривало компенсувати і які стають відправною точкою для хронічних захворювань та процесів передчасного старіння. Особливо це стосується таких захворювань цивілізації, як ішемічна хвороба серця, цукровий діабет, атеросклероз та рак. Більш того, хронічні дегенеративні захворювання центральної нервової системи, такі як хвороба Альцгеймера та хвороба Паркінсона, також пов’язані із вільними радикалами.
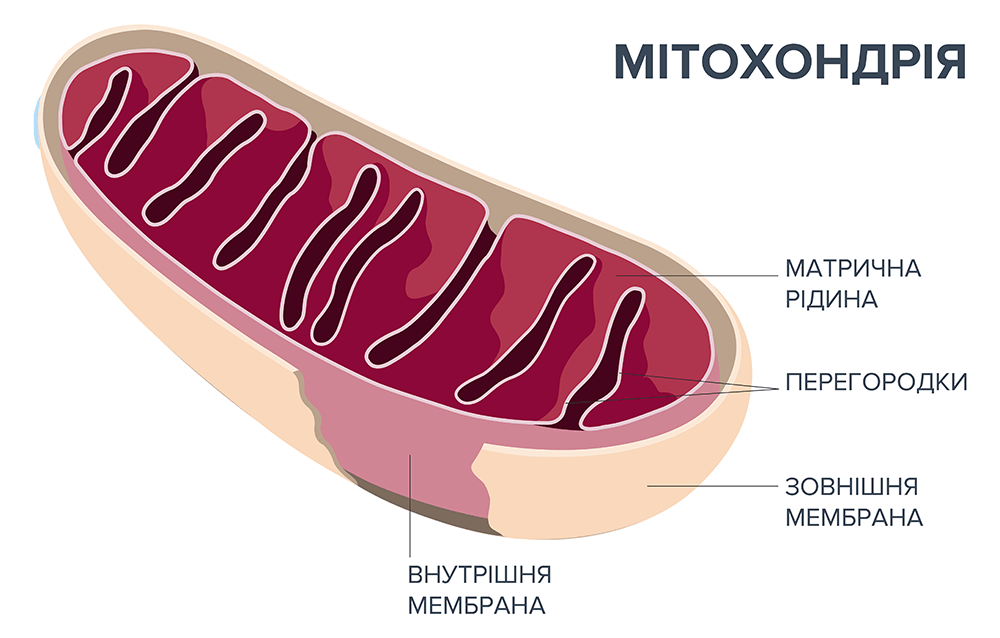
Живі системи використовують кисень повітря в якості окислювача для досягнення максимально можливого виходу енергії. Порівняння виходу енергії між безкисневим (анаеробним) виробництвом енергії та окислювальним розщепленням дає це зрозуміти на прикладі 1 моля глюкози. В той час як глюкоза за допомогою ферментації анаеробно в якості енергії поставляє тільки 2 молі АТФ, окисне розщеплення такої ж кількості цукру з використанням O2 перевищує доступну енергію приблизно в 19 разів. Значне перевищення енергетичного виходу приводить окислення в деяких фізіологічних реакціях та характеризується значним навантаженням на весь організм. Рівні активованого кисню, оскільки вони виникають в окислювальних системах, постійно викликають окисне пошкодження клітин, яке без складних антиоксидантних захисних механізмів швидко призведе до загибелі клітин.
Реактивні форми кисню (РФК “реактивні форми кисню”=ROS «reactive oxygen species»), що постійно утворюються в мітохондріях, мають особливо сильні окислювальні властивості. Вони можуть реагувати з цілим рядом біологічних субстратів (ліпіди, білки, ДНК, глюкоза) в середовищі, в якому вони утворюються. Завдяки надзвичайній реакційній здатності вільні радикали атакують майже всі структури людського організму. Структури клітинних мембран та клітинних ядер, що містять ліпіди, особливо схильні до ризику через їх хімічну структуру (множинні подвійні зв’язки). Так звані перекиси ліпідів виникають в результаті реакції між вільними радикалами та ненасиченими жирними кислотами, що знаходяться в мембранах. Вони призводять до морфологічних змін у клітинних мембранах. Цей процес погіршує функцію мембранно-зв’язаних ферментів та рецепторів та пригнічує транспорт іонів у клітинах. Порушення проникності мембран призводить до збільшення припливу кальцію, який ініціює руйнування клітини за допомогою інших механізмів.
ПОКАЗАННЯ ДО ВИКЛЮЧЕННЯ ОКСИДАТИВНОГО СТРЕСУ
• Сильне погіршення загального самопочуття
• Хронічна втома
• Виснаження
• Сильне зниження показників
• Труднощі з концентрацією уваги
• Мігрень
• Депресія
• Серцево-судинні захворювання
• Підозра на атеросклероз
• Цукровий діабет
• Порушення роботи імунної системи
• Повторні інфекції
• Алергія
• Аутоімунні хвороби
• Хвороби легенів
• Бронхіальна астма
• Емфізема легенів
• Нейродегенеративні хвороби
• Хвороба Альцгеймера
• Хвороба Паркінсона
• Аміотрофічний бічний склероз
• Забруднення навколишнього середовища
• Важкі метали
• Пестициди
• Органічні розчинники
• УФ-промені
• Високопродуктивний спорт
• Знижена функція детоксикації
• Хвороба печінки
• Порушення функції нирок
• Шлунково-кишкові розлади
ЛАБОРАТОРНА ДІАГНОСТИКА
У лабораторній діагностиці доступні ряд методів, які фіксують комплексний вплив оксидативного стресу, а також дозволяють робити висновки про стан забезпеченості антиоксидантними захисними поживними речовинами.
Методи обстеження для виявлення оксидативного стресу
PerOx
Підвищені значення пероксидів ліпідів у плазмі є наслідком перекисного окислення мембранних ліпідів та інших структур, що містять ліпіди. Визначення пероксидів (тест PerOx) – це фотометричне вимірювання, яке визначає, скільки пероксидів (окисників) циркулює в крові. Цей тест рекомендується завжди, якщо є загальна підозра на оксидативний стрес. Це скринінговий тест, який може представляти ступінь оксидативного стресу у сенсі довгострокового маркера. Підвищені значення відповідають дисбалансу між про- та антиоксидантними факторами та можуть бути виявлені відповідно до тривалості цього дисбалансу. Причинами такої ситуації є, наприклад, прозапальні процеси.
Перекисне окислення – це завжди багатофакторний процес, в якому, крім пероксидів, залучений ряд ферментів (наприклад, мієлопероксидаза або циклооксигенази) та двовалентні катіони (мідь, залізо). В принципі, на цьому етапі слід зазначити, що різні лабораторні параметри не можуть одночасно охоплювати всі окислювальні патомеханізми. Негативний результат тесту не виключає оксидативного стресу. Тому, наприклад, якщо є прооксидативні ризики або захворювання, завжди доцільна подальша діагностика (наприклад, окиснений ЛПНЩ, окислення ДНК).
Якщо під час розширеної діагностики виявляють лише підвищені значення PerOx, то можна припустити оксидативне навантаження, що, ймовірно, ще не призвело до подальших прооксидативних вторинних реакцій. Для того, щоб цього максимально уникнути, слід починати терапію антиоксидантами.
Розширені маркери оксидативного стресу
Для доповнення основної діагностики доступні додаткові спеціальні лабораторні параметри, за допомогою яких можна оцінити антиоксидантні захисні системи та будь-який оксидативний стрес. Тут також слід зазначити, що локалізація оксидативних процесів відіграє вирішальну роль. Отже, наприклад, за допомогою параметрів ДНК-окиснення виявляються особливі окислювальні процеси в ядрі клітини (але не за допомогою окисненого ЛПНЩ).
Через складність дії окисного механізму, часто необхідно проводити комбінацію специфічних лабораторних досліджень.
Окиснений холестерин ЛПНЩ (OxLDL)
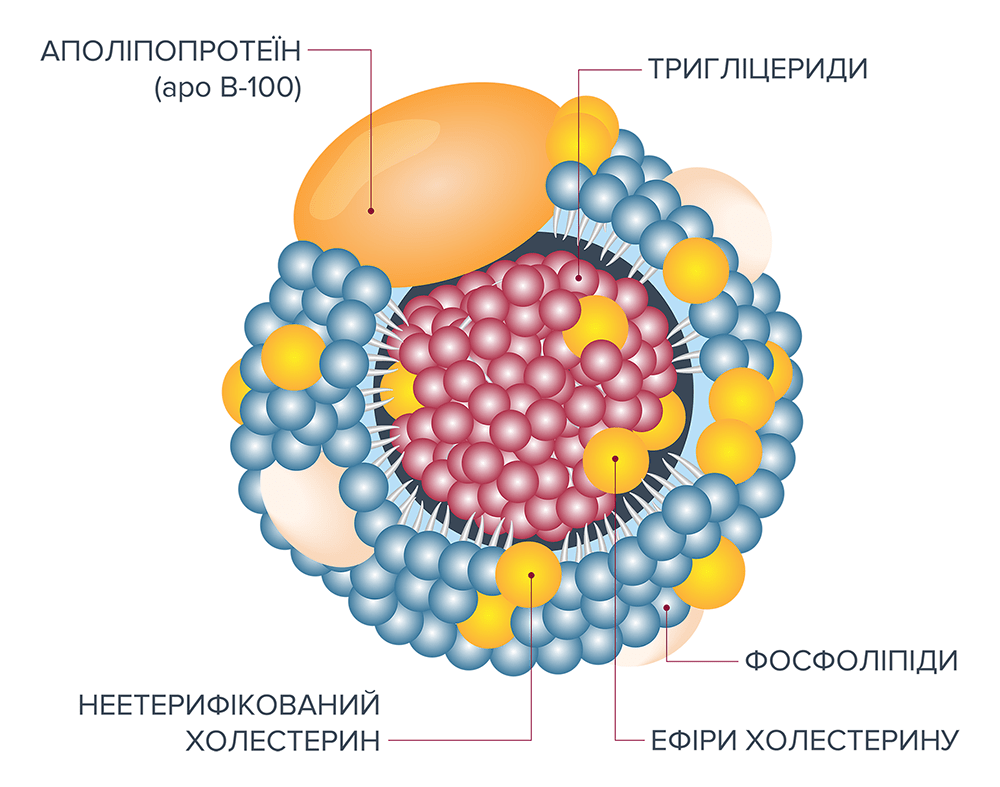
ЛПНЩ – це ліпопротеїн, який транспортує холестерин і фосфоліпіди з печінки до тканин (мал. 3). Ліпопротеїни всмоктуються в клітини за допомогою рецепторів ЛПНЩ. Якщо в плазмі висока концентрація ЛПНЩ, ліпіди, а саме аполіпопротеїн В100 можуть окислювати частки ЛПНЩ. Окислення може бути викликане різними молекулами або реакціями. Сюди входять ферменти (мієлопероксидази, ліпоксигенази та циклооксигенази), а також активні форми кисню, активні сполуки азоту або іони металів, такі як залізо та мідь. В результаті цієї модифікації (окислення) oxЛПНЩ більше не визнається як нативний ЛПНЩ і викликає аутоімунні та цитотоксичні реакції. Цей процес мобілізує додаткові імунні клітини, і моноцити дедалі більше диференціюються в макрофаги, які можуть поглинати за допомогою рецепторів, розташованих на поверхні, необмежену кількість ЛПНЩ. Макрофаги прилипають до ендотелію, перетворюються на пінисті клітини, які стають помітними у вигляді смужок жиру і є першими ознаками атеросклеротичних змін.
OxЛПНЩ має навіть вищий атерогенний потенціал, ніж ЛПНЩ, і тому може бути використаний як значущий маркер для оцінки прогресування та прогнозу атеросклеротичних бляшок. Значущість підвищеного рівня OxЛПНЩ у цьому відношенні перевершує важливість холестерину ЛПНЩ.
Окислення ДНК
Пошкодження нуклеїнових кислот (особливо тиміну та гуаніну) у разі окисних процесів в організмі має особливе значення, оскільки це може призвести до змін хромосом, а отже, і генетичного складу. Гуанін перетворюється на 8-гідроксигуанозин, який зазвичай видаляється системами відновлення ДНК. Якщо система відновлення перевантажена, 8-гідроксигуанозин накопичується, і це призводить до мутацій, які також можуть зіграти певну роль у розвитку раку. Підвищена концентрація виявляється також у літньому віці, при хронічних захворюваннях печінки, гіперхолестеринемії та / або гіпертонії, цукровому діабеті та у курців. У цих випадках звичайного надходження антиоксидантів може бути недостатньо для забезпечення належного захисту внутрішньоклітинних структур. Тому доцільно, крім оцінки будь-яких основних захворювань чи факторів способу життя, збільшити надходження внутрішньоклітинних ефективних антиоксидантів (особливо вітаміну С) і, якщо потрібно, перевірити метаболізм глутатіону. Також важливо забезпечити достатню кількість вторинних фітонутрієнтів.
Ізопростани
Ненасичені жирні кислоти особливо сприйнятливі до пошкодження радикалами кисню через їх хімічну структуру (подвійні зв’язки). Атака кисневого радикала призводить до утворення пероксидів у жирних кислотах. Ізопростани виробляються вільними радикалами в ненасиченій жирній кислоті – арахідоновій кислоті. Арахідонова кислота важлива як незамінна частина клітинних мембран. Крім того, вона впливає на активність мембранних рецепторів. Ізопростани вказують на ступінь механізму оксидативного пошкодження. Виявлення підвищеної концентрації ізопростану також дозволяє оцінити антиоксидантну здатність, а також використовується для з’ясування факторів ризику серцево-судинних захворювань, цукрового діабету, гіперхолестеринемії, ожиріння та паління.
Преаналітика (матеріал)
• PerOx – сироватка
• Окислений холестерин ЛПНЩ (OxLDL) – сироватка
• Окислення ДНК-сеча
• Ізопростани – сеча
Методи дослідження для оцінки антиоксидантного захисного механізму
Антиоксидантна здатність
Визначення антиоксидантної здатності є мірою системи антиоксидантного захисту і показує, чи можуть антиоксиданти, присутні в крові пацієнта, достатньо повністю перетворити пероксиди, додані in vitro. Тест охоплює всі антиоксидантні речовини, присутні в крові, як ендогенні та і введені з їжею. Він, таким чином, також виявляє антиоксиданти, такі як сечова кислота. Дослідження антиоксидантної здатності є корисним доповненням до тесту PerOx, описаного вище. З одного боку, можна оцінити пропускну здатність захисних систем, а з іншого боку, визнати можливе навантаження, що виникає в результаті цього.

В ідеалі обидва виміряні значення знаходяться в рівновазі, так що можна припустити, що гомеостаз не потребує терапевтичних втручань. З іншого боку, відхилення від норми (значення PerOx мають тенденцію бути високими /підвищеними, антиоксидантна здатність, як правило, низькою / зниженою), свідчать про наявність оксидативної метаболічної ситуації. У цьому випадку показана контрольована терапія заміщення.
Подальші методи дослідження для перевірки антиоксидантного захисного механізму
Для подальшої або додаткової діагностики доступні також інші окремі параметри для оцінки антиоксидантних захисних механізмів. Можна дослідити такі важливі антиоксидантні ферменти, як супероксиддисмутаза (СОД) або глутатіонпероксидаза (GPX), а також специфічні антиоксидантні мікроелементи, такі як вітаміни Е і С, кофермент Q10, альфа-ліпоєва кислота або глутатіон. Слід зазначити, що більша частина окисного стресу усувається на ферментативному рівні. Тому часто корисний додатковий генетичний аналіз.
Антиоксидантні ферменти
Супероксиддисмутаза (СОД) відповідає за елімінацію супер-оксид-аніона, першого токсичного похідного кисню. Таким чином, фермент формує першу лінію захисту від окисного стресу. Активність СОД залежить від достатнього вмісту мікроелементів міді та цинку (Cu / Zn-СОД цитозолю) та марганцю (Mn-СОД мітохондрій). Зниження рівня СОД часто пов’язано з низькою концентрацією цих мікроелементів, так що СОД також може бути визначена у сенсі «функціональної діагностики мікроелементів». Перевага такої функціональної діагностики полягає в тому, що таким чином можна визначити індивідуальні потреби пацієнта щодо відповідних мікроелементів. Основною функцією глутатіонпероксидази є усунення пероксидів ліпідів. Причиною зниженої активності глутатіонпероксидази може бути недостатнє надходження селену.
Антиоксидантні мікроелементи та пептиди
Глутатіон
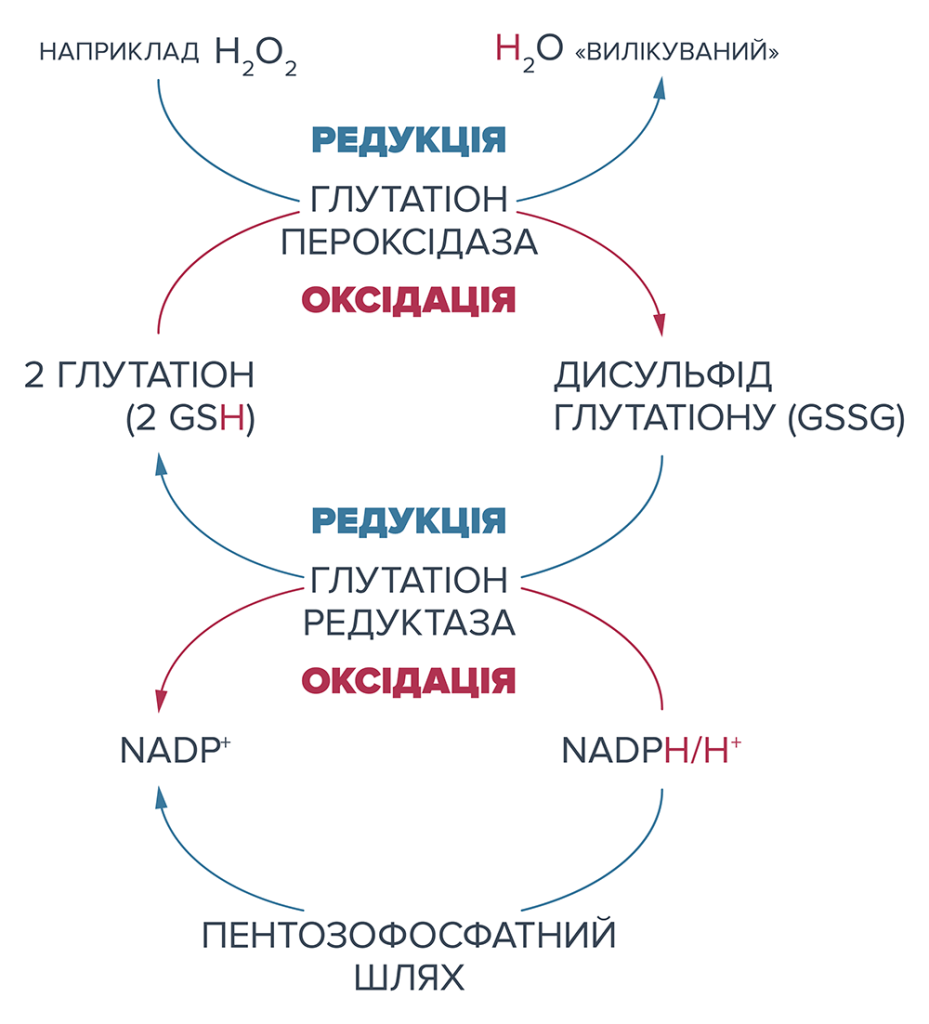
Трипептид глутатіон (GSH) утворюється з амінокислот глутаміну, цистеїну та гліцину. Крім того, весь метаболізм глутатіону залежить від достатнього надходження кофакторів, таких як вітамін С, вітамін В2 та В6, альфа-ліпоєва кислота, селен та L-карнітин. В організмі глутатіон діє в різних структурних формах в системі глутатіону, яка перевершує інші системи, що виконує безліч завдань. Зважаючи на свою антиоксидантну важливість, GSH, серед іншого, надає комплексну дію проти активованих попередників кисню та вільних радикалів, а отже, є одним із власних захисних факторів організму проти окисного стресу.
У випадку оксидативного стресу, як правило, використовується GSH. Визначення окисненого глутатіону (GSSG) та обчислення співвідношення GSH / GSSG показують ступінь оксидативного стресу. Фактор зменшується в літньому віці та особливо після інтенсивних фізичних навантажень.
Альфа-ліпоєва кислота
На додаток до своєї важливої ролі коферменту у виробництві клітинної енергії, альфа-ліпоєва кислота (ALA) відіграє центральну роль в антиоксидантній мережі. Як потужний антиоксидант, ALA інактивує вільні радикали та здатна регенерувати інші оксиданти, такі як вітаміни С та Е, кофермент Q10 та глутатіон. Її перевага перед іншими оксидантами полягає в тому, що ALA може потрапляти у всі тканини та рідини завдяки своїм водорозчинним властивостям. Крім того, ALA може перетнути гематоенцефалічний бар’єр і, таким чином, також мати захисний ефект для ЦНС.
Сірковмісні амінокислоти
Термін тіоли охоплює сірковмісні амінокислоти цистеїн, цистеїніл-гліцин та глутатіон, які разом функціонують як потужні поглиначі радикалів. Будучи носіями сірчаних груп, вони здатні реагувати із вільними радикалами, утворюючи сульфідні та дисульфідні містки й таким чином знищувати їх пошкоджувальну дію. Крім того, вони впливають на активність ключового ферменту в процесах відновлення ДНК (полі-АДФ-рибоза-полімераза). Концентрація тіолів є мірою антиоксидантного резерву в організмі. Вони також показують здатність до відновлення пошкоджень ДНК. Високий рівень тіолів вважається профілактичним фактором проти деяких захворювань та прискорених процесів старіння. Низькі концентрації вказують на ризик пошкодження ДНК та ризик розвитку атеросклерозу і пухлин.
Коензим Q10
На додаток до своєї центральної ролі в енергетичному метаболізмі як електронного носія, кофермент Q10 є потужним поглиначем радикалів завдяки своїй хімічній структурі (хінонове кільце та подвійні зв’язки в бічному ланцюзі). Завдяки своїм ліпофільним властивостям він може захищати та стабілізувати особливо чутливі системи, такі як клітинні мембрани та тканини шкіри, від перекисного окислення ліпідів. Коензим Q10 також здатний регенерувати окиснений вітамін Е.
Аскорбінова кислота
Вітамін С є важливим виловлювачем РФК (ROS) і може захищати різні біологічні субстрати (білки, жирні кислоти, ДНК) від окислення. Вітамін С також здатний запобігати окисленню ЛПНЩ, спричиненому різними РФК (ROS).
Токофероли
Завдяки своєму гідрофобному характеру вітамін Е може включатися в жирні кислоти клітинної мембрани та ліпопротеїнів, де він виконує захисну функцію та пригнічує прогресування перекисного окислення ліпідів, спричиненого оксидативним стресом. Серед токоферолів альфа- та гама-токоферол мають найсильніші антиоксидантні властивості.
Бета-каротин і вітамін А
Деякі каротиноїди, такі як бета-каротин, розщеплюються на вітамін А, який відіграє важливу роль у зорі. Більшість каротиноїдів та вітамін А реагують із синглетним киснем і можуть запобігти окисленню деяких біологічних субстратів, особливо поліненасичених жирних кислот. Окислювальні стресові ситуації базуються на багатофакторних патомеханізмах, проти яких організм намагається захиститися за допомогою складних, різноманітних механізмів. Це неминуче означає, що, з одного боку, для повноцінної діагностики слід використовувати різні лабораторні параметри, а, з іншого боку, режим терапії повинен бути таким же широким. Тому важливо, крім симптоматичної терапії на основі ліків, ініціювати причинно-наслідкові заходи, які також спрямовані на зміну способу життя та усунення факторів стресу.
Преаналітика (матеріал)
Антиоксидативна здатність – сироватка
СОД – ЕДТА
Глутатіон – ЕДТА, сироватка
Глутатіонпероксидаза – ЕДТА
Альфа-ліпоєва кислота – сироватка
Тіоли — сироватка
Рекомендації щодо терапії при оксидативному стресі
Захисні мікроелементи та ферменти
Речовини з групи вітамінів, мікроелементи, амінокислоти, вторинні фітонутрієнти та ферменти по суті служать антиоксидантами.
Вітаміни
Коензим Q10 – ЕДТА, сироватка
Вітамін С – сироватка
Вітамін Е – сироватка
Каротиноїди – сироватка
Мікроелементи в цільній крові
Мідь, марганець, селен, цинк – гепарин, ЕДТА.
Найважливішими представниками цих захисних факторів є:
• Вітаміни (А, С, Е та бета-каротин, ніацин)
• Мікроелементи, такі як залізо, мідь, марганець, селен та цинк
• Біофлавоноїди
• Відновлений глутатіон
• Альфа-ліпоєва кислота
• Мелатонін (епіфізарний гормон)
За допомогою цих речовин в організмі накопичуються або функціонують інші антиоксиданти або ферменти, наприклад:
• Глутатіон вітамін С, L-цистеїн, L-глутамін та L-гліцин
• Глутатіонпероксидаза селен, вітамін Е, рибофлавін, ніацин
• Каталази залізо
• Супероксиддисмутази цинк, марганець, мідь
Для оптимального використання захисного потенціалу груп речовин має сенс використовувати взаємодоповнюючі речовини для терапії. Наприклад, вітамін Е забезпечує захист від окислення в області ліпідовмісних структур, які знаходяться в клітинних мембранах, тоді як вітамін С має особливе відношення до цитоплазми та тим самим захищає ядро клітини. Бета-каротин, своєю чергою, діє в зоні міжклітинного простору. Вторинні фітонутрієнти, такі як каротиноїди та поліфенольні сполуки, такі як флавоноїди, ресвератрол та антоціани, є важливими для потужної антиоксидантної терапії. Отже, оптимальний антиоксидантний статус можна підтримувати завдяки регулярному вживанню відповідних продуктів харчування.
| Сполучення | Продукти з високим вмістом |
| Вітамін С | Свіжі фрукти та овочі |
| Вітамін Е (токофероли, токотрієноли) | Рослинні олії |
| Поліфенольні антиоксиданти (ресвератрол, флавоноїди) | Чай, кава, соя, фрукти, оливкова олія, какао, кориця, орегано, червоне вино, гранат, ягоди аронії |
| Каротиноїди | Фрукти, овочі, яйця |

Комбінація антиоксидантних речовин має сильніший ефект, ніж окрема речовина