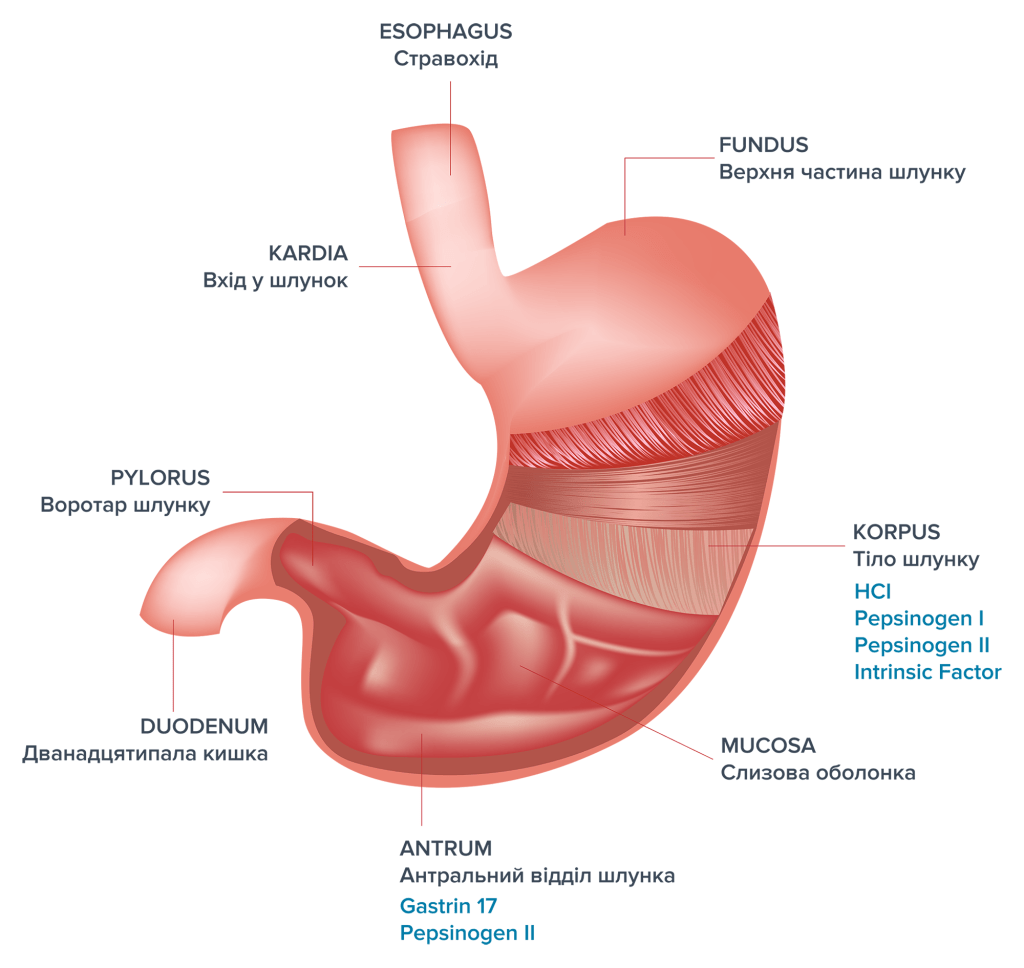
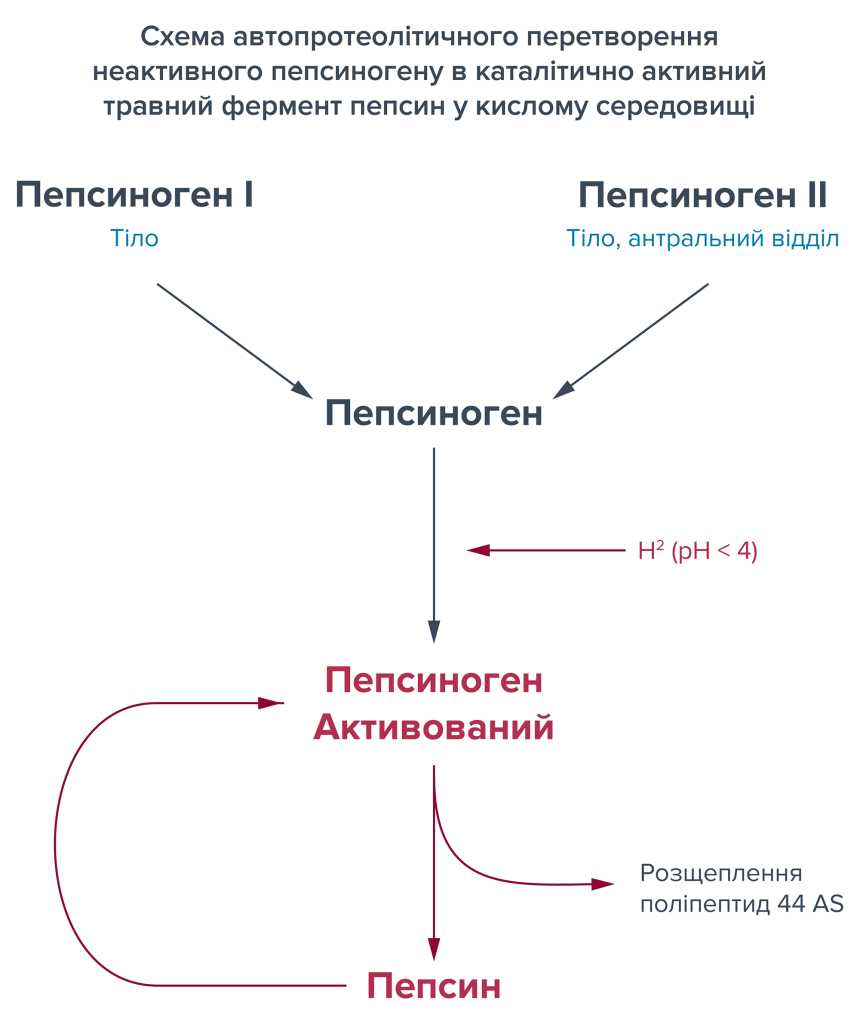
Шлунок виконує ряд важливих завдань для ефективного перетравлення поживних речовин у кишківнику. Після того, як їжа була подрібнена і виділена слина в ротовій порожнині, додаткові травні ферменти – часто у вигляді неактивних попередників – додаються до харчової суміші (наприклад, пепсиногени) і завдяки перистальтичним рухам шлунку добре змішуються до гомогенного стану. Оскільки протеолітичні травні ферменти мають оптимальний ефект у кислому середовищі, вміст шлунку підкислюється соляною кислотою (HCl).
Багато харчових компонентів (білки та клітковина) є складними молекулами й тому важко перетравлюються. Завдяки індукованій кислотою денатурації (руйнуванню третинної структури) цих молекул, створюються кращі можливості для ферментативного травлення. Секреція шлункового соку також має дезінфекційну дію. Більшість патогенів, таких як бактерії, віруси та інші мікроорганізми, знищуються низьким значенням pH. Крім того, до харчової суміші в шлунку додається специфічний транспортний глікопротеїн (внутрішній фактор, Intrinsic Factor) для ефективного всмоктування вітаміну В12 з їжі в кишківнику.
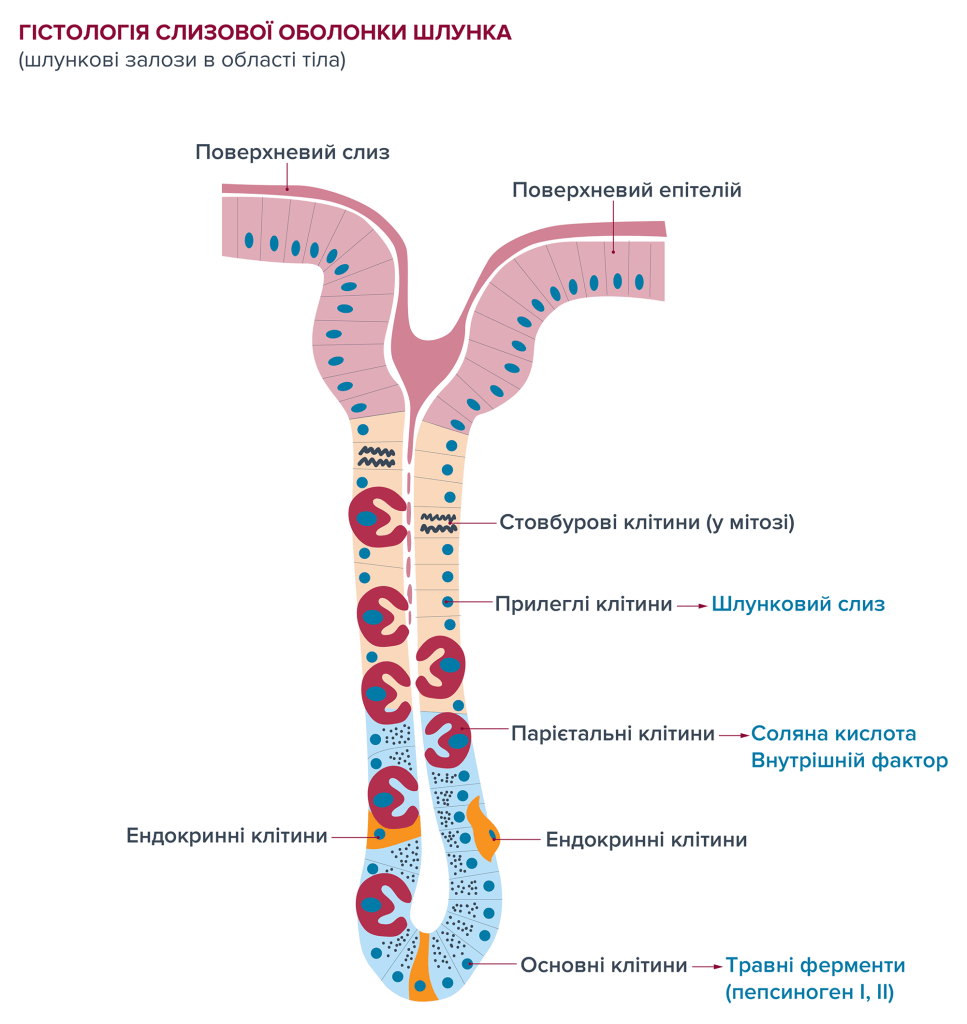
Стінка шлунку складається з багатьох шарів. У слизовій оболонці шлунку, внутрішньому шарі органу, є шлункові залози, які складаються з різних типів клітин і відкриваються в просвіт шлунку. Секреція шлункового соку основними клітинами (травні ферменти) та парієтальними клітинами (соляна кислота, внутрішній фактор), а також вироблення шлункового слизу вторинними клітинами відбувається головним чином у слизовій оболонці тіла та дна шлунку. Слиз, яка покриває слизову оболонку тонкою плівкою, служить насамперед для захисту шлунку від самоперетравлення агресивним шлунковим соком і для захисту від патогенних мікроорганізмів. Кількість шлункового соку або шлункової кислоти, що виділяється залежить від виду та кількості споживаної їжі. Деякі харчові продукти (наприклад, кава, нікотин, спеції), зокрема, стимулюють утворення кислоти.
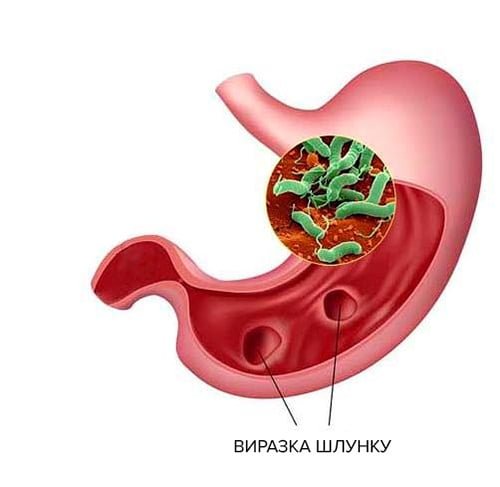
Слизова оболонка шлунку, кровообіг та імунний захист утворюють функціональну одиницю, яка називається бар’єром слизової оболонки. Слизова оболонка перебуває в постійній трансформації (нарощуванні та руйнуванні клітин) і зазвичай швидко відновлюється після пошкодження. Але якщо функція порушена або послаблення чи пошкодження занадто сильні, це може призвести до запалення слизової оболонки.